Application Note 創薬におけるクローンスクリーニング用
ハイスループットIgG定量
- 96サンプルを15分以内に測定可能な、迅速・均一・自動化対応のアッセイです
- 少量のサンプルと最小限の前処理で、粗マトリックス中のサンプル解析が可能です
- 2.5~2000 mg/Lの範囲でIgGを正確に測定できます
PDF版(英語)
Cathy Olsen博士|Sr.アプリケーションサイエンティスト|モレキュラーデバイス
Hannah Byrne博士|生物製剤部門責任者|バリタセル社
はじめに
バイオ医薬品は、製薬業界で最大かつ最も急速に成長している分野であり、売上は5,000億ユーロ、年間成長率は8%です。臨床試験や市場投入のいずれの場合でも、バイオ医薬品候補の製造プロセスはすべて細胞株開発から始まります。モノクローナル抗体(mAb)は、主要なバイオ医薬品治療モダリティとして確立されています。堅牢な製造プラットフォームの構築は、抗体創薬の取り組みを臨床および商業的成功へと円滑に移行させるための鍵です。mAb(例:IgG)タイターの正確かつ信頼性の高い測定は、すべてのバイオ医薬品の生産において最適な細胞培養性能を確保するため、開発およびその後の製造に不可欠です(図1)。バイオプロセス全体でタンパク質タイターをリアルタイムで確実にモニタリングできる能力は、オペレーターが最大のタンパク質産出を得るためにプロセス条件を迅速に調整し、プロセス時間を最小化することを可能にします。タイターデータへの迅速なアクセスは、下流工程の準備に関する早期の意思決定も可能にし、生産タイムラインをさらに短縮します。
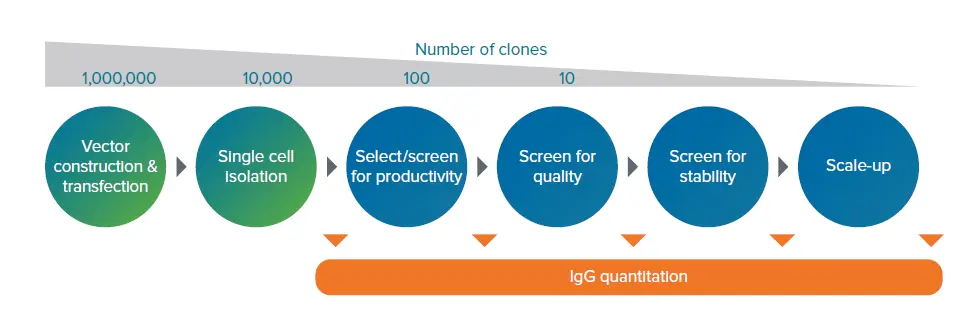
図1. 細胞株開発プロセス:細胞導入からスケールアップまで。細胞株の生成プロセスは非常に複雑で手間がかかり、時間も要します。高い生産性、長期的な安定発現、良好な製品品質を持つクローンは稀であるため、バイオ医薬品製造のすべての段階でスクリーニング戦略が実施されます。治療効果を持つ新しいmAbの開発において最も遅いステップはクローン選択であり、これは現在、従来のスクリーニング技術によって妨げられています。さらに、現在のワークフローは単機能で高コスト、専門的なトレーニングを必要とします。
バイオ医薬品業界でmAbを定量するために現在使用されているさまざまな技術の中で、ゴールドスタンダードであるProtein A HPLC、バイオレイヤー干渉法、ELISA、免疫比濁法が一般的です。これらはすべて、テストあたりのコスト、ハードウェアのコスト、実験を実行するために必要なスタッフの経験など、異なる特徴を持っています。重要なのは、これらの技術の一部は、全細胞、細胞破片、汚染物質を除去するための遠心分離や希釈など、解析前に複数のステップを必要とすることです。業界で広く採用されているにもかかわらず、高コスト(Protein A HPLC)、細胞汚染に対する感度による結果のばらつき、ヒューマンエラーの影響、労力を要するワークフロー(ELISA)、および結果取得までの時間の長さ(場合によっては3時間以上)は、Protein A HPLCやELISAをバイオプロセス全体でIgG定量に採用しようとするユーザーにとって大きな障壁となっています。
ここでは、ValitaCell社のValitaTiter IgG定量アッセイと、モレキュラーデバイスの蛍光偏光(FP)対応マイクロプレートリーダーを組み合わせた、完全に最適化された迅速・堅牢・高精度なIgGタイタープラットフォームの概要を紹介します。ValitaTiterアッセイの測定範囲は、2.5~100 mg/Lまたは100~2000 mg/Lで、シンプルな「添加して読み取る」プロトコールを採用しています。ValitaTiterプレートは、蛍光標識されたターゲット特異的プローブで予めコーティングされており、ユーザーはIgG試料を添加する前に再構成します。アッセイは15分以内に実施でき、96ウェルまたは384ウェルプレートフォーマットでバイオプロセスワークフローに組み込むことが可能です。アッセイはハイスループットで完全自動化が可能です。解析は、最大10×10⁶ cells/mLを含む粗細胞培養液中で、少量のサンプルと最小限の前処理で実施できます。検出は、モレキュラーデバイスのマイクロプレートリーダー(SpectraMax® iD5、i3x、Paradigm®、M5マルチモードマイクロプレートリーダー)で蛍光偏光を用いて行います。(i3xおよびParadigmプレートリーダーには蛍光偏光検出カートリッジが必要です。)
SpectraMaxマルチモードマイクロプレートリーダーは優れた柔軟性を提供し、ほとんどのモデルには吸光度、蛍光、発光が含まれ、蛍光偏光(FP)、時間分解蛍光(TRF)、FRETの構成オプションがあります。さらに、ウエスタンブロット、細胞イメージング、迅速なキネティクス用インジェクターなどのアップグレード可能なモジュールも利用できます。
| Valita®TITER | Surface interferometry | ELISA | HPLC | |
|---|---|---|---|---|
| 総アッセイ時間 [96 サンプル] | <15分未満;30分未満 | 55-65分 | 6時間以上 | 25-45時間 |
| サンプル量 [μL] | 5-30 | 180+ | 100 | 1000-2000 |
| 測定範囲 [mg/L] | 2.5-100; 100-2000 | 0.025-2000 | 0.5-5 | >10 |
| 精密度 | <2mP | <5% | <5-10% | <2% |
| 細胞混入に対するロバスト性 | 10 x 10⁶ million cells/mL |
分析前に細胞を除去 | 分析前に細胞を除去 | 分析前に細胞を除去 |
| オートメーション・フレンドリー | Yes | No | Yes | No |
表1. Valita®TITERと競合製品の主要特長の概要
アッセイ原理
ValitaTiterおよびValitaTiter Plusは、蛍光標識されたProtein G誘導体を用いてIgG-Fc相互作用を定量する迅速かつハイスループットなアッセイであり、検出には蛍光偏光(FP)を使用します。FPは分子サイズの変化を効果的に解析します(図2)。「固定化」された蛍光体は偏光光で励起され、同じ偏光面で光を優先的に放出します。光子の吸収と放出の間に分子が回転することで、光の偏光が「ねじれる」現象が生じます。小さな分子は溶液中で大きな分子よりも速く回転します。したがって、蛍光標識されたFc特異的プローブが結合することによる分子サイズの変化は、光の脱偏光度合いによって検出できます。蛍光標識されたIgG結合ペプチドが未結合の場合、それは急速に回転し、IgG(約20倍大きい)に結合した場合よりも光を強く脱偏光します。FPの検出は、溶液を偏光光で励起し、励起光に対して平行(偏光成分)および垂直(脱偏光成分)の両方の面で放出光強度を測定することで行います。FPは通常、2つの強度の正規化差として表され、単位はミリ偏光単位(mP)です。
材料
- ValitaCell ValitaTiter Kit
- ValitaCell ValitaTiter Plus Kit
- Sigma IgG standard (Sigma)
- XP Media™ CHO Growth A(モレキュラーデバイス)、4 mM L-グルタミン添加
- SpectraMax iD5® マルチモードマイクロプレートリーダー
- 蛍光偏光フィルター485 nm BW 25 nm垂直偏光300nm~750nm 2枚セット(モレキュラーデバイス)
- 蛍光偏光フィルター535 nm BW 25 nm垂直偏光300nm~750nm 2枚セット (モレキュラーデバイス #6590-0137)
- SpectraMax i3x マルチモードマイクロプレートリーダー
- 蛍光偏光(FP-FLUO)検出カートリッジ(モレキュラーデバイス #0200-7009)
- SpectraMax Paradigmマルチモードマイクロプレートリーダー
- 蛍光偏光(FP-FLUO)検出カートリッジ(モレキュラーデバイス)
- SpectraMax M5マルチモードマイクロプレートリーダー
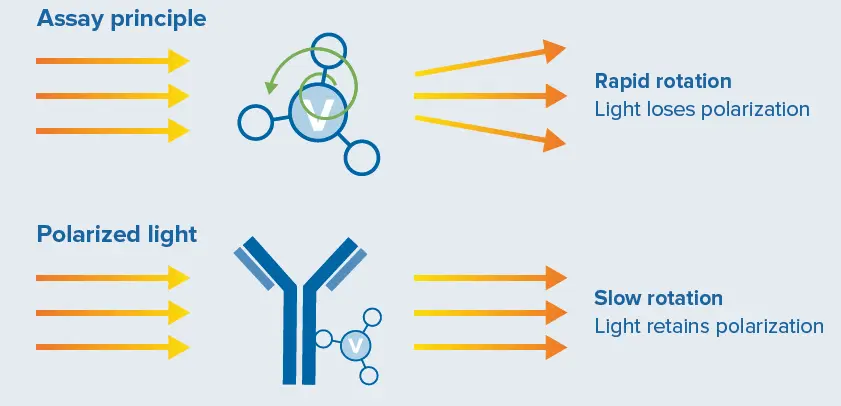
図2. アッセイは蛍光偏光を用いてFcを含むIgGを定量します。小さな未結合分子は溶液中で急速に回転し(上)、大きな結合分子はゆっくり回転します(下)。
方法
- IgG標準の段階希釈をXP Media/L-グルタミンを希釈液として行い、濃度は2.5~100 mg/L(ValitaTiter)または100~2000 mg/L(ValitaTiter Plus)としました。
- ValitaTiterまたはValitaTiter Plusプレートの各ウェルに60 µLの培地を分注し、プローブを再構成しました。
- 次に、調製した標準液60 µLを適切なウェルに添加しました。
- ウェル内容物は、ピペッティングで上下に3回穏やかに混合しました(アッセイワークフローの概要は図3参照)。
- アッセイプレートは測定前に室温で暗所にてインキュベートしました(ValitaTiterは5分、ValitaTiter Plusは15分)。測定はモレキュラーデバイス社のマイクロプレートリーダーで行い、最適化された設定は表2(ValitaTiter)および表3(ValitaTiter Plus)に示します。
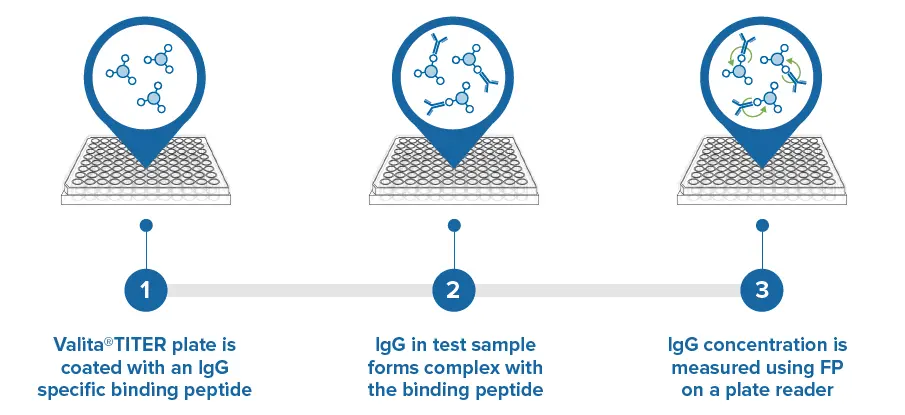
図3. アッセイプレートの各ウェルは蛍光標識されたFc特異的プローブで予めコーティングされています(1)。IgGサンプルがプローブに結合します(2)。結合は蛍光偏光で測定されます(3)。
| セッティング | iD5 | i3x | M5 | Paradigm |
|---|---|---|---|---|
| 測定モード | 蛍光偏光 | 蛍光偏光 | 蛍光偏光 | 蛍光偏光 |
| 励起 | 485 nmモノクロメーター | 485nm | 485 nm | 485nm |
| エミッション | 535 nmフィルター | 535nm | 525 nm,515 nm カットオフ | 535nm |
| PMTゲイン | Low | -- | Medium | -- |
| Gファクター | 1.0 | 1.0 | 1.0 | 1.0 |
| Attenuation | なし | -- | -- | -- |
| Integration time or flashes | 400 ms | 400ms | 100 flashes/read | 400nm |
| 読み取り高さ (mm) | 3.6 | 4.8 | -- | 4.1 |
| セトリング時間 (ms) | -- | -- | 100 | -- |
表2. モレキュラーデバイスのマイクロプレートリーダーでValita®TITERアッセイの蛍光偏光測定を行うための最適設定。SpectraMax i3xおよびParadigmプレートリーダーにはFP-FLUO検出カートリッジが必要です。不要な設定は「---」で示します。
| セッティング | iD5 | i3x | M5 | Paradigm |
|---|---|---|---|---|
| 測定モード | 蛍光偏光 | 蛍光偏光 | 蛍光偏光 | 蛍光偏光 |
| 励起 | 485 nmモノクロメーター | 485nm | 485 nm | 485nm |
| エミッション | 535 nmフィルター | 535nm | 525 nm,515 nm カットオフ | 535nm |
| PMTゲイン | Low | -- | Low | -- |
| Gファクター | 1 | 1 | 1 | 1 |
| Attenuation | 1 OD | -- | -- | -- |
| Integration time or flashes | 400 ms | 400ms | 100 flashes/read | 400nm |
| 読み取り高さ (mm) | 5.5 | 5.2 | -- | 4.8 |
| セトリング時間 (ms) | -- | -- | 100 | -- |
表3. モレキュラーデバイスのマイクロプレートリーダーでValita®TITER Plusアッセイの蛍光偏光測定を行うための最適設定。SpectraMax i3xおよびParadigmプレートリーダーにはFP-FLUO検出カートリッジが必要です。不要な設定は「---」で示します。
結果
ValitaCellのValitaTiterアッセイをモレキュラーデバイスのマルチモードマイクロプレートリーダーで使用するための最適パラメータを特定し、創薬および開発におけるハイスループットIgG定量プラットフォームを提供するための検証を行いました。IgG標準曲線は、サンプルやプレートの前処理や洗浄ステップを必要としないシンプルな「添加して読み取る」方法で調製・解析され、容易なワークフローを実現しました。
SpectraMax iD5プレートリーダーを用い、励起に485 nm FPフィルターセット、蛍光検出に535 nm FPフィルターセットを使用した場合、優れた結果が得られました。IgG標準(ValitaTiterは2.5~100 mg/L、ValitaTiter Plusは100~2000 mg/L)は、全範囲で高い線形性(R²=0.99)を示しました(図4)。ValitaTiter(表4)およびValitaTiter Plusアッセイ(表5)について、SpectraMax i3x、Paradigm、M5プレートリーダーでも同様のデータが得られました。SoftMax® Proソフトウェアの事前設定済みプロトコールにより、mP計算と曲線プロットが自動化されました。
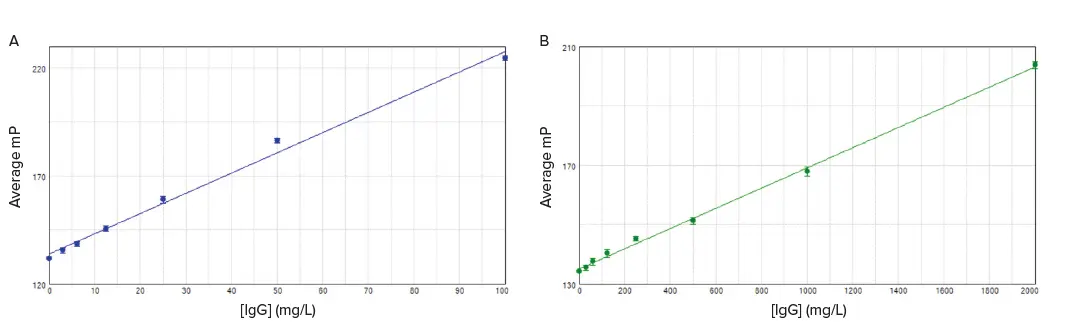
図4. ValitaTiter(A, r²=0.993)およびValitaTiter Plus(B, r²=0.998)アッセイの標準曲線。SoftMax Proソフトウェアで線形フィットを用いてプロットしました。
| iD5 | i3x | M5 | Paradigm | |
|---|---|---|---|---|
| デルタ mP | 93 | 70 | 80 | 89 |
| 平均StDev (mP) | 1.12 | 2.12 | 0.57 | 0.82 |
| 平均%CV | 0.7 | 0.7 | 0.5 | 0.3 |
| 最大StDev | 1.54 | 3.53 | 1.06 | 1.27 |
| 最大%CV | 1.0 | 1.3 | 1.0 | 0.4 |
表4. モレキュラーデバイスのプレートリーダーで読み取ったValita®TITER標準のΔmP、平均標準偏差(StDev)、および%CV(n=4)。
| iD5 | i3x | M5 | Paradigm | |
|---|---|---|---|---|
| デルタ mP | 69 | 85 | 92 | 88 |
| 平均StDev (mP) | 1.05 | 3.54 | 1.63 | 1.14 |
| 平均%CV | 0.7 | 1.3 | 1.6 | 0.4 |
| 最大StDev | 1.59 | 6.49 | 2.26 | 1.43 |
| 最大%CV | 1.1 | 2.0 | 2.4 | 0.5 |
表5. モレキュラーデバイスのプレートリーダーで読み取ったValita®TITER Plus標準のΔmP、平均標準偏差(StDev)、および%CV(n=4)。
結論
mAb IgG titerの正確かつ信頼性の高い測定は、すべてのバイオ医薬品の生産において最適な細胞培養性能を確保するため、開発およびその後の製造に不可欠です。時間とリソースの最小限の投資で正確な結果を得られるアッセイは、成功にとって重要です。本検証では、ValitaTiterアッセイとモレキュラーデバイスのマイクロプレートリーダーを組み合わせることで、広い機能範囲にわたるIgG定量が可能であることを実証しました。
ValitaTiterアッセイは、サンプルの前処理や精製ステップを必要とせず、粗サンプル中のIgGを正確かつ迅速に定量できる均一なハイスループット手法です。この96ウェルアッセイは、SpectraMax iD5プレートリーダーおよびFP検出を備えたその他のモレキュラーデバイス製マイクロプレートリーダーで完全に検証され、信頼性の高い結果を保証します。SoftMax Proソフトウェアは、検出のセットアップ時間を最小化し、標準曲線フィッティングとサンプル定量を自動化します。
PDF版(英語)