アプリケーションノート
SpectraMax iD5 マイクロプレートリーダーを用いた 高感度デュアルレポーターアッセイによる
NF-κB 活性化のモニタリング
利点
- 高感度なデュアルレポーターアッセイ
- 内部コントロールに対するレポーター発現の標準化により、測定結果の正確性が向上
- SoftMax Proソフトウェアにプリセットされているプロトコルにより、データの取得から解析までを迅速に処理
SpectraMax iD5マルチモードマイクロプレートリーダーについて問い合わせる
はじめに
レポーター遺伝子は、多様なシグナル伝達経路や病態に関わる遺伝子の代わりとして用いられ、遺伝子発現の研究にとって重要なツールです。ルシフェラーゼは最も一般的なレポーター遺伝子です。その理由はルミノメーターや発光マイクロプレートリーダーで容易に検出できる点や、細胞内の発光バックグラウンドが低く、高感度なアッセイが可能な点にあります。ルシフェラーゼは、通常、対象とする遺伝子の発現を検出するために用いられます。一方、ウミシイタケRenilla reniformis に由来するルシフェラーゼは、多重化ルシフェラーゼアッセイにおける第2 のレポーターとして用いられ、トランスフェクション効率や細胞生存率などのサンプル間のばらつきを標準化するために使用されます。
SpectraMax® DuoLuc™ Reporter Assay Kit を用いると、哺乳動物細胞におけるホタルルシフェラーゼおよびウミシイタケルシフェラーゼの発現を高感度に定量できます。2 種類の最適化された検出試薬を順次分注することで、同一のマイクロプレートウェルにおいて両方のルシフェラーゼの活性を測定できます。このアッセイでは、恒常的に発現するコントロールレポーター(ウミシイタケルシフェラーゼ)のシグナルを用いて試験レポーター(ホタルルシフェラーゼ)のシグナルを標準化することができます。
アッセイキットは、SmartInject ™テクノロジー搭載のインジェクターシステムを備えたSpectraMax® iD5 マルチモードマイクロプレートリーダーによる測定に最適化されています。
このアプリケーションノートでは、DuoLuc Reporter Assay Kit とSpectraMax iD5を用いて、哺乳動物細胞モデルにおけるNuclear Factor-κB(NF-κB)の活性化を検出する方法について説明します。NF-κBは種々の細胞プロセスにおいて遺伝子発現を調節する主要な転写因子で、炎症、免疫、細胞分化、細胞増殖、アポトーシスなどの多くの現象に関与しています。腫瘍壊死因子Tumor necrosis factor α(TNF-α)のようなシグナリング分子は、NF-κB 抑制分子を分解し、NF-κB を核移行できるようにするシグナル伝達経路を活性化します。
これにより、多数の遺伝子が調節されます(図1) 1。NF-κB のシグナル伝達経路の阻害は、多発性硬化症、糖尿病、アルツハイマー病などの非常に多くの疾患に関連しており、NF-κB シグナル伝達経路の理解を深める手段は極めて重要です。
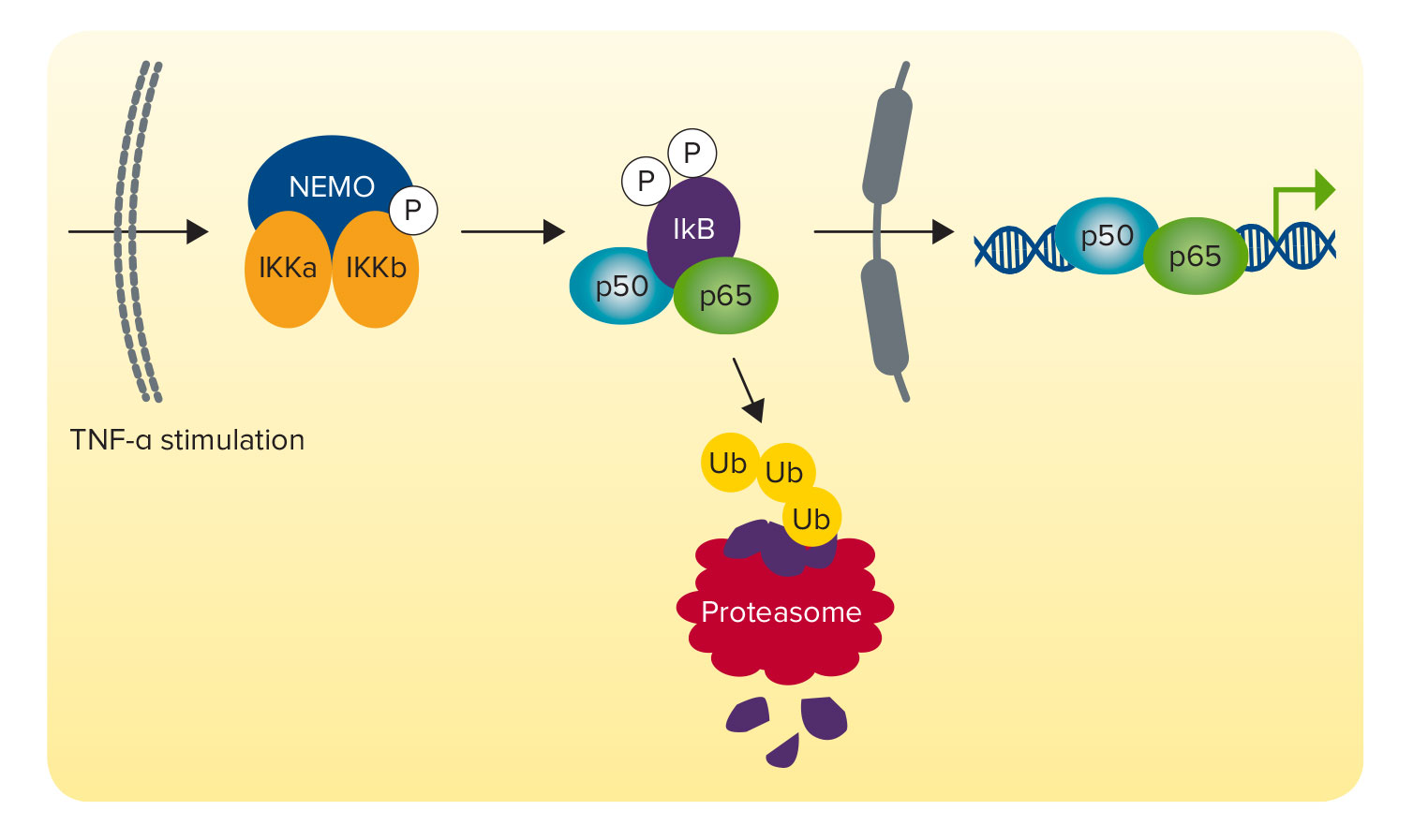
図1. NF-κB シグナル伝達経路
TNF-α は、シグナル伝達経路を活性化することでNF-κB のインヒビターIκB を分解し、NF-κB 転写因子の核移行を促進します。
材料
- SpectraMax DuoLuc Reporter Assay Kit(Molecular Devices、#R8361)
- HEK293 細胞(ATCC、#CRL-1573)
- 細胞培養培地(10% FBS/DMEM、ペニシリン/ ストレプトマイシン含有)
- pGL4.32[luc2P/NF-κB-RE/Hygro] ホタルルシフェラーゼベクター(Promega、 #E849A)
- pGL4.75[hRluc/CMV] ウミシイタケルシフェラーゼベクター(Promega、#E693A)
- FuGENE HDトランスフェクション試薬(Promega、#E2311)
- Opti-MEM | Reduced Serum Media(ThermoFisher Scientific、#31985062)
- 96 ウェルクリアボトムポリスチレンTC 処理済み白色マイクロプレート(Corning、#3610)
- TNF-α/PBS 溶液(10 μg/mL、1 mg/mL BSA)(Sigma、#T0157)
- BrightMax White Sealing Film(Excel Scientific、#WT-50)
- SpectraMax iD5 マルチモードマイクロプレートリーダー
- SmartInject テクノロジー搭載インジェクターシステム
方法
細胞のトランスフェクション
細胞密度80% のHEK293 細胞をトリプシン処理によって回収し、96 ウェルクリアボトム白色プレートに15,000 cells/wellとなるように播種しました。細胞密度が50% 以上に達した後、NF-κB-RE ホタルルシフェラーゼベクターとウミシイタケコントロールベクターをコトランスフェクションしました。その際、FuGENE とDNA の混合液を、3 種類の異なる比率で調製しました(表1)。その後、細胞を37° C のインキュベーターで24 時間培養しました。
TNF-α による誘導
10 μg/mL のTNF-α 溶液を培地を用いて20 ng/mL に希釈し、誘導溶液を調製しました。対照実験には培地のみを使用しました。細胞を培養したサンプルプレートから培地を除去し、対照溶液または誘導溶液100 μL を各ウェルに添加しました。プレートをインキュベーターに戻し、7 時間誘導しました。
細胞溶解液の調製
TNF-αで刺激したサンプルプレートから培地を除去し、PBS で細胞を1 回洗浄しました。Passive Lysis Buffer を室温に戻し、各ウェルに20 μL 添加しました。細胞の溶解は、室温で15 分間ゆっくり撹拌しながら行いました。発光シグナルを最大化するため、プレート底部に白色のプレートシールを貼り付けました。
ルシフェラーゼアッセイの手順
キットのすべての構成品を室温で解凍しました。ホタルルシフェラーゼ基質凍結乾燥品1 バイアル2.2 mg に、水220 μL を加え、ホタルルシフェラーゼ基質原液(以下、ホタル基質原液)を調製しました。同様に、Aquaphile セレンテラジン凍結乾燥品1 バイアル440 μg に、水220 μL を加え、ウミシイタケルシフェラーゼ基質原液(以下、ウミシイタケ基質原液)を調製しました。
ホタルルシフェラーゼ基質溶液(以下、ホタル基質溶液)は、ホタル基質原液をキットのFirefly Assay Buffer で50 倍希釈して調製しました。ウミシイタケルシフェラーゼ基質溶液(以下、ウミシイタケ基質溶液)は、ウミシイタケ基質原液をキットのRenilla Assay Buffer で50 倍希釈して調製しました。96 ウェルプレート1 枚に対して、それぞれの基質原液220 μL を希釈して、11 mL の基質溶液を調製しました。
SoftMax® Proソフトウェアにプリセットされているプロトコルを使用して、次の手順でデータ取得と解析を行いました。
- 1. インジェクター1 を用いて、ホタル基質溶液100 μL をウェルに添加。
- 2. 遅延時間2 秒間。
- 3. 積算時間5 秒間で、ホタルルシフェラーゼ反応の発光を測定。
- 4. インジェクター2 を用いて、ウミシイタケ基質溶液100 μL をウェルに添加。
- 5. 遅延時間2 秒間。
- 6. 積算時間5 秒間で、ウミシイタケルシフェラーゼ反応の発光を測定。
- 7. それぞれのウェルについて、1 回目の測定(ホタルルシフェラーゼ)のRLU 値を2回目(ウミシイタケルシフェラーゼ)の測定値を用いて標準化。
SmartInject テクノロジーを搭載したSpectraMax iD5 インジェクターシステムは、試薬のインジェクション中にアッセイプレートを撹拌し、効率的に試薬を混合することで、シグナルを最大化できます。
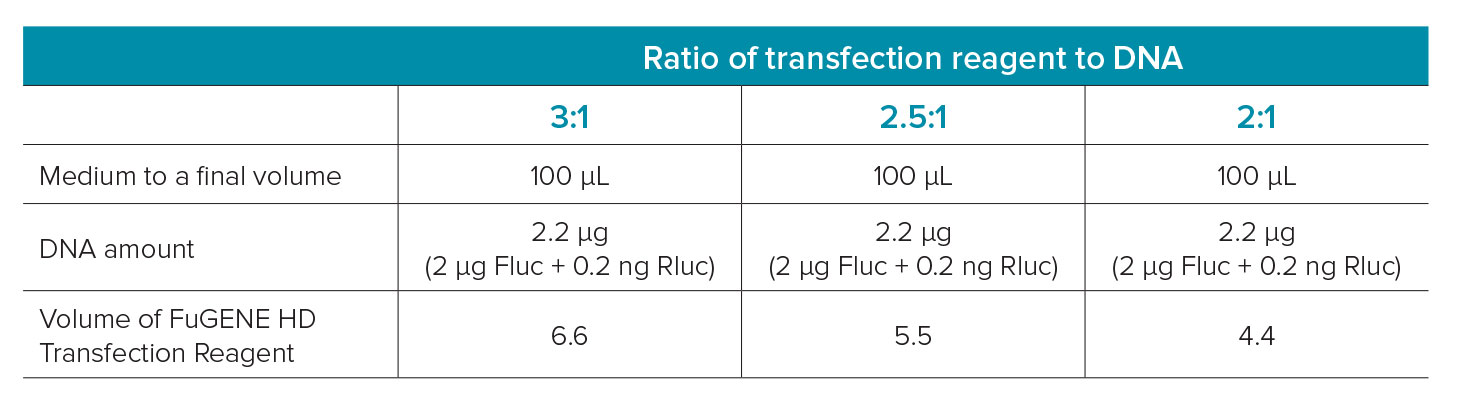
表1. トランスフェクション試薬の量およびDNA 量
結果
いずれのトランスフェクション条件においても、ウミシイタケルシフェラーゼの発現レベルは高く、TNF-αで誘導してもそのレベルに変化はあまり見られませんでした。一方、ホタルルシフェラーゼの発現レベルはサイトカインであるTNF-α による誘導によって顕著に上昇しました(図2)。全体的には、ルシフェラーゼの発現は、試薬とDNA の比率が2:1 の場合に他の比率よりも低い結果となりました。
ホタルルシフェラーゼの発光シグナルをウミシイタケルシフェラーゼの発光シグナルで標準化すると、実施したトランスフェクションの3 種類の条件すべてで、TNF-αによって発現が強く誘導されることがわかりました(図3)。トランスフェクション試薬とDNA の比率が3:1 および2.5:1 の条件において、標準化された発光シグナルが相対的に低値である一方、TNF-α 誘導による発光シグナルの変化率は相対的に高値でした。表2 では、TNF-α での誘導による発光シグナル変化率をトランスフェクション条件別に示しています。発光シグナル変化率は、トランスフェクション試薬とDNA の比率が2.5:1 のときに最大になりました。
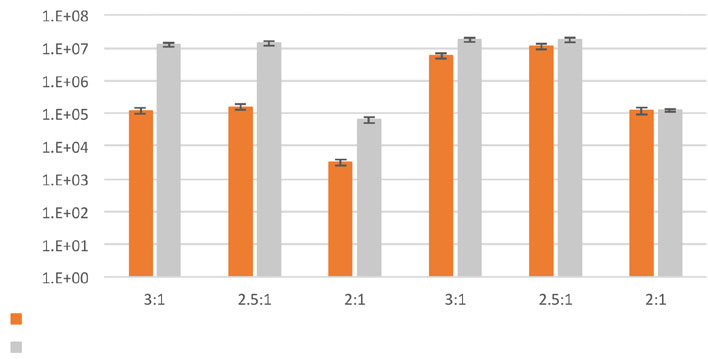
図2. ルシフェラーゼ発光のRLU 値
発光強度(RLU)を非誘導細胞とTNF-α 誘導細胞についてトランスフェクション条件(試薬: DNA 比)別に示した。各トランスフェクション条件につきN=9 で測定を実施。
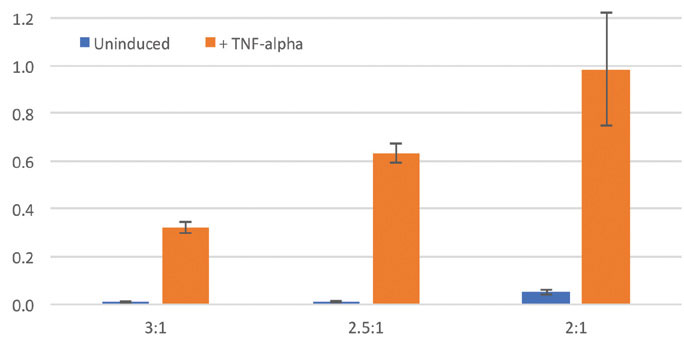
図3. 標準化されたルシフェラーゼの発光シグナル
ホタルルシフェラーゼのRLU 値をウミシイタケルシフェラーゼのRLU 値を用いて標準化した。
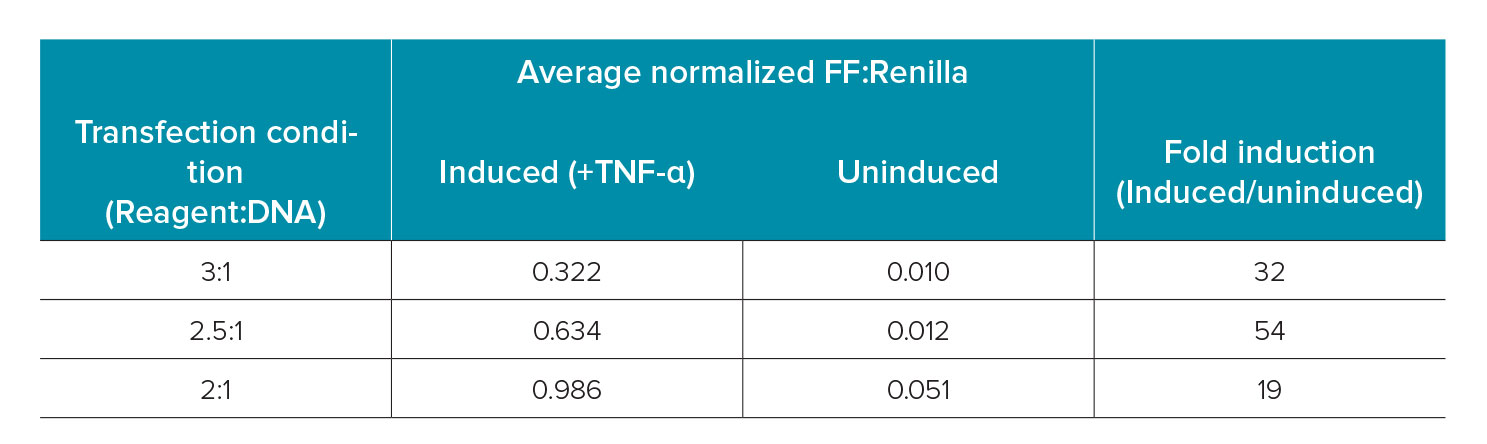
表2. トランスフェクション条件別の発光シグナル変化率
トランスフェクション試薬とDNA の比率が2.5: 1 のとき、誘導による発光シグナルの変化率が最大になった。
SpectraMax DuoLuc Reporter Assay Kit は、SmartInject テクノロジー搭載のインジェクターシステムを備えたSpectraMax iD5 プレートリーダーに最適化されています。SoftMax Pro ソフトウェアにプリセットされたキット専用のアッセイプロトコルでデータの取得と解析が簡素化
するとともに、迅速で高感度かつ信頼性の高いデュアルルシフェラーゼアッセイが可能です。
結論
DuoLuc Reporter Assay Kit を用いたレポーターアッセイによって、HEK293 細胞において、TNF-α によるNF-κB 応答配列による顕著な誘導が実証されました。このアッセイは、ホタルルシフェラーゼおよびウミシイタケルシフェラーゼのいずれについても感度が良く、ともに大きな発光シグナルが得られました。実施した条件の中では、TNF-α により、最大54 倍のNF-κB 応答配列の誘導が観察されました。
SpectraMax iD5マルチモードマイクロプレートリーダーについて問い合わせる
参考文献
- Oeckinghaus, A and Ghosh, S. The NF-κB Family of Transcription Factors and Its Regulation. Cold
Spring Harb Perspect Biol. 2009 Oct; 1(4): a000034.
