アプリケーションノート
自動細胞イメージングシステムを用いた
アポトーシスの解析
利点
- シンプルな洗浄不要のホモジニアスアッセイを用いてアポトーシスを評価
- 画像取得と同時進行で解析が可能で、迅速に結果を取得
- プリセット解析プロトコルを用いて、細胞の状態をモニターしアポトーシスを定量化
このページは、自動翻訳ツールを用いて制作されているため、正確でない表現が含まれている可能性があります。原文は下記よりダウンロードできます。
ImageXpress Pico自動細胞イメージングシステムについて問い合わせる
はじめに
アポトーシスは多細胞生物でおこるプログラムされた細胞死です12 。その過程では生化学的事象を通して、アポトーシスに特有な細胞形態の変化と細胞死がおこります。形態学的変化には、細胞の収縮、核の断片化、クロマチン凝縮、染色体DNAの断片化、およびmRNA分解が含まれます。
アポトーシスは高度に調節された過程であり、飢餓、感染、低酸素、酸化ストレスなどを含む種々のストレッサーへの応答として、内因性経路を介して開始されます。ミトコンドリア損傷はアポトーシスの開始に重要な役割を果たします。外因性経路では、腫瘍壊死因子(TNF)受容体ファミリーを介したシグナル伝達などの外部シグナルによって開始されます。どちらの経路もカスパーゼ酵素を活性化することによって細胞死を誘導します。アポトーシスの調節における細胞死は、癌を含む種々の疾患に関与しています。
このアプリケーションノートでは、自動細胞イメージングシステムを用いたアポトーシス検出のための細胞ベースのアッセイについて説明します。
材料
- HeLa細胞(ATCC P/N CCL-2)
- 培地
- DMEM:CellGro L-glutmaine(Corning)
- 10% FBS(BenchMark™;Gemini P/N 100-106)
- 1%ペニシリン/ストレプトマイシン
- スタウロスポリン(Sigma P/N S5921)
- マイトマイシンC(Sigma P/N M4287)
- カンプトテシン(Sigma P/N C9911)
- EarlyTox Caspase-3/7 NucView 488 アッセイキット (Molecular Devices P/N R8348)
- 96ウェル、黒、クリアボトムマイクロプレート(Greiner P/N 655090)
- ImageXpress Pico 自動細胞イメージングシステム、およびCellReporterXpress画像取得・解析ソフトウェア
ワークフロー

方法
ヒト子宮頸癌細胞株であるHeLa細胞を、ウェル当たり5,000細胞で、黒色、クリアボトム、96ウェルのマイクロプレートに播種し、37°C、5% CO2で一晩培養しました。翌日、アポトーシスを誘導するため、細胞を異なる濃度の抗癌化合物-スタウロスポリン、マイトマイシンCまたはカンプトテシン-で4回ずつ処理しました。各化合物の最高濃度は、スタウロスポリン10μM、マイトマイシンC 200μM、カンプトテシン100μMでした。18時間後、細胞をEarlyTox™ Caspase-3/7 NucView 488色素およびエチジウムホモダイマー IIIで30分間染色し、最終的な濃度をそれぞれ5μMおよび3μMとなるようにしました。次いで、ヘキストを各ウェルに6μMの最終濃度で添加し、37°C、5% CO2で15分間インキュベーションしました。
Caspase-3/7 NucView 488アッセイキット
カスパーゼ3とカスパーゼ7は、アポトーシスの実行段階で活性化されるプロテアーゼです。EarlyToxキット由来のカスパーゼ3/7NucView488基質を用いて、細胞内のカスパーゼ3/7活性を検出します。この基質はカスパーゼ-3/7 DEVD認識配列と、それに連結されたDNA染色蛍光色素からなります。最初は非蛍光性で、細胞膜を透過して細胞質に入ります。アポトーシス細胞では、この基質はカスパーゼ-3/7に切断され、細胞核に移動して高い親和性でDNAに結合する色素が放出されます。500nmでの励起にて、530nmでの明るい緑色蛍光をもたらし、カスパーゼ活性化のレベルを評価するために使用することができます。全細胞数の評価にはヘキスト33342核染料を、死亡細胞数(外膜が破壊された細胞)の評価にはエチジウムホモダイマーを用いました。
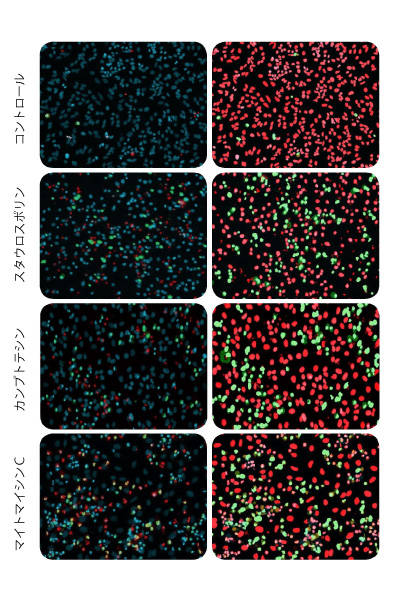
図1.自動細胞イメージングを用いたアポトーシスの検出
HeLa細胞を抗癌化合物で処理。各画像の細胞に使用された化合物濃度は、0.3μMスタウロスポリン、66μMカンプトテシン、および22μMマイトマイシンC。細胞はヘキスト、エチジウムホモダイマーIII、EarlyTox Caspase-3/7 NucView 488 アッセイキットを用いて染色。 左パネル:ヘキストによる核染色は青色、アポトーシス核は緑色、死細胞核は赤色。 右パネル:アポートシス解析マスク。アポトーシス核(緑色)および非アポトーシス核(赤)。
自動細胞イメージングによるアポトーシスの評価
染色後の細胞をImageXpress Pico自動細胞イメージングシステムを用いて、10X対物レンズで撮影しました。画像は1ウェルあたり1か所ずつ、DAPI、FITCおよびTexasRedチャネルを用いて、それぞれ20、500、50 msの露光時間で撮影しました。図1は、コントロール細胞と0.3μMスタウロスポリン、66μMカンプトテシン、および22μMマイトマイシンCで処理した細胞の画像を示しています。ヘキストによる核染色は青色、アポトーシス核は緑色、死細胞核は赤色で示されています。 CellReporterXpress画像取得・分析ソフトウェアに搭載のアポトーシス解析プロトコルを用いて、画像取得と同時進行で解析を行い、カスパーゼ染色によって示されるアポトーシス細胞の数および割合を評価しました。さらに、エチジウムホモダイマー染色は、死細胞の数および割合を検出するため、ヘキスト染 色は全細胞を規定するためにしました。アポトーシスの誘導について得られた濃度応答曲線を、測定されたEC 50値とともに図2に示します。アポトーシスの強力な誘導物質として知られているキナーゼ阻害剤スタウロスポリンのEC50は、異なる細胞機構(生体内還元性アルキル化)を介して抗癌作用を示すマイトマイシンCのEC50よりも約100倍低い数値となりました。
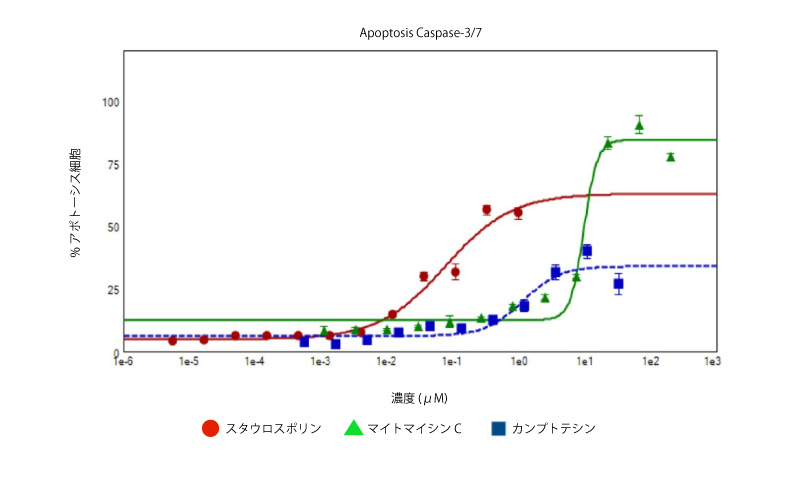
図2. 3種類の抗がん化合物に対する濃度反応曲線
アポトーシス細胞の割合: スタウロスポリン (赤EC50 0.076μM)、マイトマイシンC(緑、EC50 9.669μM)およびカンプトテシン(青色、EC50 1.14μM)
まとめ
ImageXpressPico自動細胞イメージングシステムと付属のCellReporterXpress画像取得・解析ソフトウェアを使用することによりプリセット解析プロトコルを用いて簡単かつ迅速にアポトーシスの評価と定量ができました。 またEarlyToxアッセイキットは、疾患の研究、抗癌剤の評価、細胞の健康状態のモニタリングに有用であると考えられます。
このページは、自動翻訳ツールを用いて制作されているため、正確でない表現が含まれている可能性があります。原文は下記よりダウンロードできます。
ImageXpress Pico自動細胞イメージングシステムについて問い合わせる
参考文献
- Green, Douglas (2011). Means to an End: Apoptosis and other Cell Death Mechanisms. Cold Spring Harbor, NY: Cold Spring Harbor Laboratory Press. ISBN 978-0-87969-888-1.
- Alberts, Bruce; Johnson, Alexander; Lewis, Julian; Raff, Martin; Roberts, Keith; Walter, Peter (2008). Molecular Biology of the Cell. (5th ed.). Chapter 18. Apoptosis: Programmed Cell Death Eliminates Unwanted Cells. Garland Science. p. 1115. ISBN 978-0-8153- 4105-5.
- Karam, Jose A. (2009). Apoptosis in Carcinogenesis and Chemotherapy. Netherlands: Springer. ISBN 978-1-4020-9597-9
- Verweij J1, Pinedo HM. Mitomycin C: mechanism of action, usefulness and limitations. Anticancer Drugs. 1990 Oct;1(1):5-13.
